- Accueil
- L’association
- Pourquoi Birmania and Co ?
- Bureau et infos
- Chartes
- Adresses des éleveurs
- Demande de diplôme
- Demande d’affixe
- Adhésion
- Spéciales d’élevage
- RESULTATS SPECIALE D’ELEVAGE SACRE DE BIRMANIE 10 NOVEMBRE 2024
- RESULTATS SPECIALE D’ELEVAGE SACRE DE BIRMANIE 26 NOVEMBRE 2023
- RESULTATS SPECIALE D’ELEVAGE SACRE DE BIRMANIE 13 FEVRIER 2022
- RESULTATS SPECIALE D’ELEVAGE SACRE DE BIRMANIE 12 MAI 2019
- RESULTATS SPECIALE D’ELEVAGE SACRE DE BIRMANIE 18 NOVEMBRE 2018
- RESULTATS SPECIALE D’ELEVAGE SACRE DE BIRMANIE 1ER OCTOBRE 2017
- RESULTATS SPECIALE D’ELEVAGE SACRE DE BIRMANIE 5 NOVEMBRE 2017
- RESULTATS SPECIALE DE RACE LILLE 11 DECEMBRE 2016
- RESULTATS SPECIALE DE RACE LILLE 13 DECEMBRE 2015
- Nos magazines
- Le Birman
- Autres races
- Soins et santé
- Les maladies
- Allergies du Chat
- L’alopécie
- Les antiparasitaires
- La bordetellose
- Calicivirose féline
- La Cardiomyopathie hypertrophique
- Chlamydiose
- Directives de vaccination des chiens et des chats
- Epilepsie
- Giardiose
- Hemobartonella feline
- Herpès félin
- Hypervitaminose
- Infertilité du chat
- La leucose féline
- La Rage
- La teigne
- La vaccination
- Maladies génétiques
- La metrite
- Monorchidie
- Pathologie en collectivité
- La PIF
- La PKD
- Conférences
- Génétique
- Les groupes sanguins chez les chats
- Recensement groupe sanguin
- Groupe AB
- La génétique des couleurs chez le chat
- Tares génétiques
- Tares génétiques – Défaut reproduction birman
- Les autres alopécies généralisées héréditaires
- Morphologie du chat
- Les tests de résistance à la péritonite infectieuse féline (FIPR)
- Lexique
- Identification génétique
- Du phénotype à la biologie moléculaire – couleur chat
- Le gène O
- Génétique couleur – Gène b et dilution
- Consanguinité
- Le gene I
- Les robes félines les motifs tabby
- Comportement
- Le comportement maternel
- Chats : quand rien ne va plus
- Le deuil et le chat
- Fleurs de Bach le Châtaigner
- Folie avérée
- L’intelligence du chat
- Le chat d’appartement et les doudous
- Le chat et la hiérarchie
- Le chat étranger comprend t-il notre langue ?
- LE PICA
- Le sevrage psychosocial : kézako ?
- Les fleurs de Bach
- Le marquage territorial
- Témoignage comportement
- Le chaton
- Choisir un chaton de race
- Gestation et mise bas
- Premières heures de vie : les gestes à faire
- Préparer la mise bas : un moment privilégié
- Stérilisation précoce
- La pathologie néonatale du chaton
- Intérêts de la pesée
- Donner un médicament
- Falbala de Beit Shemesh
- Le tremblement chez le chaton nouveau-né
- Point et température
- Formalités
La PKD
ANTAGENE – LABORATOIRE DE RECHERCHE ET D’ANALYSES EN GÉNOMIQUE ANIMALE
Immeuble Le Meltem
2, allée des Séquoias
69760 Limonest – France
Tél : 33 (0)4 37 49 90 03 – Fax : 33 (0)4 37 49 04 89 – www.antagene.com – antagene@antagene.com
ANTAGENE a mis au point un test ADN de dépistage de la PKD
Note d’information scientifique et technique – Novembre 2004
Par l’équipe d’ANTAGENE composée de chercheurs spécialisés en génétique moléculaire, génomique animale, et génétique des populations Le laboratoire ANTAGENE est spécialisé en génomique animale et travaille depuis 3 ans sur les maladies génétiques les plus graves pour la santé ou le bien-être du chien ou du chat. Le principal objectif est de mettre au point et de commercialiser des tests ADN fiables pour dépister ces pathologies héréditaires.
Description de la PKD
La polykystose rénale (PKR) ou polycystic kidney disease (PKD) est une maladie génétique fréquente chez différentes races de chat, notamment le Persan et les races apparentées. Les signes cliniques correspondent à ceux d’une insuffisance rénale chronique : dépression, léthargie, perte d’appétit voir anorexie, vomissements, polyurie, polydypsie, perte de poids.
Cette pathologie se traduit par le développement progressif de kystes dans les reins, par la destruction du tissu rénal, par une insuffisance rénale pouvant provoquer la mort prématurée de l’animal. Le rythme de croissance des kystes rénaux est très variable d’un chat à l’autre.
Le dysfonctionnement rénal apparaît alors plus ou moins tardivement entre 2 et 10 ans avec une moyenne à 7 ans. Un chat touché par la PKD peut vivre de nombreuses années sans montrer aucun signe clinique.
Transmission autosomale dominante de la PKD
La polykystose rénale est une maladie monogénique (implique un seul gène) et se transmet selon un mode autosomal (non lié au sexe) dominant.
Trois situations sont possibles :
• le chat porte deux copies normales du gène : il ne développe pas la maladie et ne transmet pas l’anomalie génétique à sa descendance,
• le chat hétérozygote porte une copie normale et une copie défectueuse du gène (mutation responsable de la maladie): il développe la maladie plus ou moins précocement et transmet l’anomalie génétique à la moitié de sa descendance,
• aucun chat portant deux copies défectueuses du gène n’a été observé à ce jour: il semble que cet état soit létal durant le développement embryonnaire.
Statistiquement, la proportion de chatons sains et atteints dans la descendance varie en fonction du statut des reproducteurs :
• croisement « sain x sain » : 100% de chatons sains,
• croisement « sain x atteint » : 50% de chatons sains et 50% de chatons atteints,
• croisement « atteint x atteint » : 33% de chatons sains, 67% de chatons atteints.
Recherches sur la PKD
ANTAGENE a développé son propre test ADN pour dépister la polykystose rénale chez le chat, à partir de l’homologue du gène PKD1 chez l’homme. Nos travaux de recherche ont mis en évidence
une seule anomalie génétique (ou mutation) associée à la maladie. Nous avons alors mis au point un test expérimental (appelé bêta-test). Entre juin et octobre 2004, ce bêta-test a été validé sur une population européenne de plus de 500 chats.
Aucun résultat individuel n’a été communiqué aux propriétaires des chats avant que l’ensemble des prélèvements soit analysés et que la précision et la fiabilité du test soient évaluées. Ce travail de validation a permis de confirmer l’existence d’une seule anomalie génétique associée à la PKD, d’exclure pour l’instant l’existence d’une autre forme génétique de la maladie, puis de définir la précision et la fiabilité du test ADN au niveau d’une population significative de chats en Europe. Nos données ont également été confrontées à celles obtenues par le laboratoire qui travaille sur la PKD au sein de l’Université de Californie à Davis aux Etats-Unis.
Précision du test ADN
La précision définit ce que le test ADN est capable de détecter. Pour la PKD et dans l’état actuel des connaissances suite à la campagne de validation, une seule forme génétique de la PKD est présente dans la population européenne de chats, c’est-à-dire qu’une seule forme défectueuse du gène explique les cas de PKD analysés.
Nous ne pouvons cependant pas exclure définitivement l’existence d’une éventuelle autre forme défectueuse du gène (ou d’un autre gène) qui provoquerait la maladie ou une maladie très proche.
Néanmoins, si une autre forme génétique de la PKD existait, elle serait rare puisqu’elle n’a pas été observée parmi les 579 chats analysés lors de la validation du test.
Fiabilité du test ADN
Pour définir la fiabilité du test, nous avons évalué la proportion de faux-positifs (test ADN positif alors que le chat est sain pour la PKD) et de faux-négatifs (test ADN négatif alors que le chat est atteint de PKD).
Parmi les 579 chats analysés, nous avons sélectionné les chats examinés par des vétérinaires spécialisés en échographie et en imagerie médicale et avons retenu les 60 chats pour lesquels nous possédons une copie des résultats d’échographie certifiés par le vétérinaire échographiste. Parmi ces 60 chats, tous les chats négatifs en échographie sont négatifs avec le test ADN (chats sains) et tous les chats positifs en échographie (présence de kystes rénaux) sont positifs avec le test ADN (chats atteints).
La fiabilité du test est donc théoriquement de 100%. Nous estimons cependant que statistiquement le nombre de faux-positifs et de faux-négatifs est compris entre 0 et 1 chat parmi 60 chats, soit une fréquence moyenne de 0,83%, soit une fiabilité supérieure à 99% (100%-0,83%=99,17%)
Nous invitons les éleveurs de chats à nous communiquer une copie des résultats d’échographie afin d’affiner notre estimation de la fiabilité du test ADN.
Prévalence de la PKD
Le tableau ci-dessous mentionne, pour chaque race, les résultats de la campagne de validation et de dépistage conduite par ANTAGENE : le nombre de chats analysés, le nombre de chats atteints (présentant l’anomalie génétique), la fréquence dans la race ; ainsi que d’autres données sur la prévalence de la PKD.
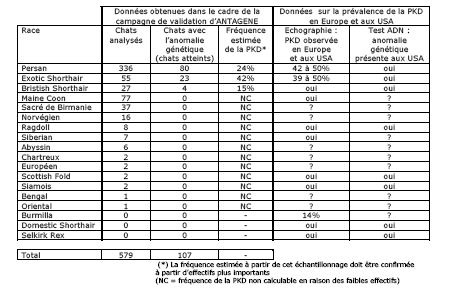
L’anomalie génétique responsable de la PKD a été découverte dans 3 races de chats en Europe : le Persan, l’Exotic Shorthair, le British Shorthair. En revanche, l’anomalie génétique n’est pas été observée chez les autres races de chats. À l’exception du Maine Coon et du Sacré de Birmanie, le manque de données ou le faible nombre de chats testés ne permettent pas de conclure sur la présence ou l’absence de cette anomalie génétique dans chacune de ces races.
Expression variable de la PKD
Dans le cadre de cette étude, nous confirmons la variabilité d’expression de la PKD. Un chat atteint (test ADN positif) peut développer les premiers kystes rénaux tardivement (après 2 ans) et présenter les premiers symptômes tardivement (parfois après 10 ans). Ce chat présente une forme légère de PKD, mais transmettra tout de même l’anomalie génétique à sa descendance : les chatons peuvent développer une forme plus grave de PKD avec un développement précoce de kystes rénaux et une insuffisance rénale prématurée.
Recommandations face à une maladie génétique : Comme pour toute maladie génétique chez le chien ou le chat, nous invitons les éleveurs à ne pas reproduire les animaux porteurs ou atteints de l’anomalie génétique afin de limiter l’incidence de la pathologie héréditaire dans la race.
Il est cependant très important de distinguer plusieurs situations en fonction de la fréquence de la maladie dans une race donnée (voir dans une lignée) :
• inférieure à 1% : la maladie est rare
• entre 1 et 10% : la maladie est fréquente
• supérieure à 10% : la maladie est très fréquente.
Dans tous les cas, il faut éviter de reproduire des animaux porteurs ou atteints d’une maladie génétique. Mais l’élimination de l’anomalie génétique doit toujours se faire progressivement sans augmenter la consanguinité et sans exclure de la reproduction des lignées entières de reproducteurs, au risque sinon de mettre en danger la diversité génétique de la race et de voir émerger d’autres maladies génétiques.
Un animal porteur ou atteint peut exceptionnellement être conservé pour la reproduction :
• à condition que l’anomalie génétique soit fréquente ou très fréquente dans la race (ou la lignée),
• à condition de le croiser avec un animal sain,
• à condition qu’il présente des qualités intéressantes pour l’amélioration de la race (morphologie, caractère, capacités de travail, etc),
• à condition de surveiller la descendance et de sélectionner absolument les descendants sains.
Recommandations spécifiques à la PKD
La situation de la PKD est particulièrement grave car il s’agit d’une maladie dominante (tout chat porteur de l’anomalie génétique est malade) et d’une maladie extrêmement fréquente chez le Persan et l’Exotic Shorthair.
Pour toutes les races présentant une fréquence de PKD inférieure à 10%, il est impératif d’exclure de la reproduction les animaux atteints. En revanche, chez le Persan, l’Exotic Shorthair (et dans une moindre mesure chez le British Shorthair), il convient d’être extrêmement vigilant. Une sélection intensive et trop rapide contre la PKD pourrait avoir de graves conséquences se traduisant par :
• la perte de certains caractères améliorateurs pour la race,
• la perte d’une diversité génétique indispensable à l’adaptation à long-terme de toute population animale,
• un risque d’augmenter la consanguinité conduisant inévitablement à l’émergence d’autres maladies génétiques.
Par conséquent, dans les races ou les lignées au sein desquelles la PKD est très fréquente, il est capital de prendre en compte tous les critères dont dispose l’éleveur et de ne pas exclure aveuglement tous les chats atteints de PKD : le remède serait vraiment pire que le mal.
Un exemple à ne pas suivre
La gangliosidose est une maladie monogénique récessive qui touchait le Chien d’eau portugais aux Etats-Unis. Un test, développé à la fin des années 1980, avait alors permis d’estimer la fréquence de porteurs à 9%. Étant donné la fréquence de cette maladie, il était recommandé de ne pas exclure de la reproduction les chiens porteurs qui présentaient par ailleurs des qualités intéressantes pour la race et à condition de les croiser avec des chiens sains.
Les éleveurs ont tout de même exclu de la reproduction tous les chiens porteurs et ont sélectionné des chiens provenant d’une lignée ne portant pas cette anomalie génétique responsable de la gangliosidose.
Malheureusement, cette nouvelle lignée était porteuse d’une autre maladie génétique, l’atrophie de la rétine. La sélection intensive pour cette nouvelle lignée a rapidement fait augmenter à 35% la fréquence de chiens porteurs d’atrophie de la rétine dans la race.
Les éleveurs ont donc remplacé une maladie génétique assez fréquente (gangliosidose, 9%) par une autre maladie génétique très fréquente (atrophie de la rétine, 35%) qui sera beaucoup plus difficile à éradiquer. L’émergence de l’atrophie de la rétine aurait pu être évitée en conservant des chiens porteurs de gangliosidose, à condition de les croiser avec des chiens sains et de surveiller la descendance. La gangliosidose aurait été éradiquée aussi efficacement par le remplacement progressif (en quelques générations) des chiens porteurs par leurs descendants sains ayant conservé les qualités des reproducteurs.
Références bibliographiques
Beck C, Lavelle RB
Feline polycystic kidney disease in Persian and other cats: a prospective study using ultrasonographyAust Vet J. 2001 Mar;79(3):181-4
Barthez PY, Rivier P, Begon D
Prevalence of polycystic kidney disease in Persian and Persian related cats in France J Feline Med
Surg. 2003 Dec;5(6):345-7
Lyons LA, Biller DS, Erdman CA, Lipinski MJ, Young AE, Roe BA, Qin B, Grahn RA.
Feline polycystic kidney disease mutation identified in PKD1 J Am Soc Nephrol. 2004
Oct;15(10):2548-55 Bell JS
The epidemiology of defective genes, and its effect on genetic counseling recommendations in pure-bred populations
Advances in canine and feline genomics, Utrecht, Oct 2004
Même s’il y a un test génétique, le plus rassurant c’est de faire des échographies pour connaître le statut de son animal.
LE BOIS DE L'EPOT
18360 SAINT VITTE
06.61.87.48.53
association@birmania-and-co.com
Retrouvez-nous sur Facebook
Club de race au LOOF
Association loi 1901 crée le 22/4/06 | JO du 3/6/06 n° 20060022-1568
Site déclaré à la CNIL le 27/04/2006, n° 1165444
Le site de BIRMANIA AND CO appartient et est géré par BIRMANIA AND CO MAG • Site créé en 05/2005 | Refonte en 03/2023 par Heavncha Studio
